Tahukah kamu bagimana bentuk molekul senyawa kima? Bentuk suatu molekul sangat penting untuk diketahui. Terdapat berbagai macam bentuk molekul yang menyusun senyawa kimia. Jika kalian belum tahu bentuk bentuk molekul senyawa kimia, pada kesempatan kali ini kami akan berbagi tentang bagaimana bentuk molekul senyawa kimia.
Maka dari itu mari kita simak pembahasan lengkapnya pada artikel tentang kimia yang sudah kami rangkum berikut ini.
Pengertian Bentuk Molekul
Tahukah kamu apa pengertian molekul? Molekul adalah gabungan dari dua macam atom atau lebih yang berada di dalam satu susunan tertentu dan terikat oleh gaya kimia. Bentuk molekul dapat bervariasi, disebabkan atom atom yang saling berikatan dan membentuk berbagai macam senyawa atau jenis molekul yang berbeda beda agar dapat stabil. Bentuk molekul biasanya berdasarkan dengan jumlah pasangan elektron terikat (PEI), pasangan elektron bebas (PEB) dan juga domain elektron.
Untuk bagaimana cara mengetahui PEI, PEB dan Domain elektron kalian dapat menggunakan struktur lewis sebagai langkah awal untuk menentukan geometri molekul. Struktur ini menggambarkan keadaan elektron valensi ydari atom yang sudah berpasangan dan berikatan secara kovalen.
Tipe Bentuk Molekul
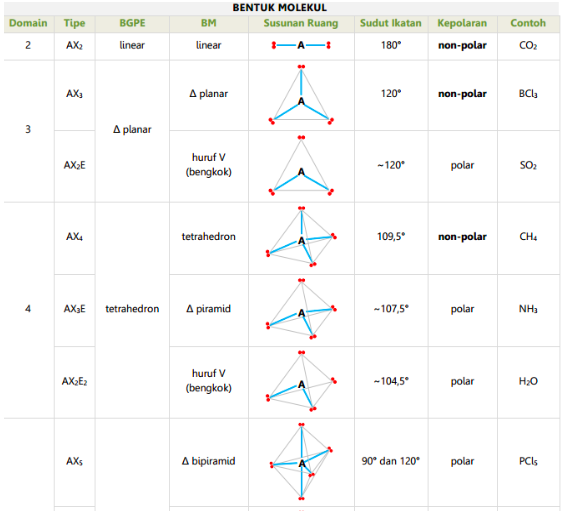 Varian bentuk sutau molekul bisa bermacam macam, seperti linear, trigonal, hingga tetrahedral. Untuk menentukan bentuk suatu molekul bisa didapatkan dari hasil percobaan struktur elektronnya.
Varian bentuk sutau molekul bisa bermacam macam, seperti linear, trigonal, hingga tetrahedral. Untuk menentukan bentuk suatu molekul bisa didapatkan dari hasil percobaan struktur elektronnya.
Teori Bentuk Molekul
Teori yang membahas terkait dengan bentuk suatu molekl terbagi menjadi tiga antara lainnya yaitu Teori VSEPR (Valence Shell Electron Pair Repulsion), Teori Hibridisasi dan Teori Domain Elektron. Berikut ini adalah penjelasan terkait ketiga teori tersebut.
Teori VSEPR
Teori yang pertama akan kita bahas yaitu VSEPR yaitu pasangan elektron yang mandiri akan saling tolak menolak, Pasangan elektron lebih cenderung saling berjauhan satu sama lainnya. Prinsip dari Teori VSEPR antara lainnya adalah sebagai berikut :
- Semakin mengecil jarak antar kedua pasangan elektron maka gaya tolak menolak akan semakin menguat
- Gaya tolak menolak akan menguat pada saat sudut di antara pasangan tersebut 90 derajat.
- Tolakan melibatkan pasangan elektron tunggal menjadi lebih kuat dibandingkan dengan pasangan ikatan : pasangan mandiri dan pasangan mandiri > pasangan mandiri dan pasangan ikatan > pasangan ikatan dan pasangan ikatan.
Teori Domain Elektron
Selanjutnya teori yang kedua akan kita bahas yaitu teori domain elektron. Berdasarkan teori domain elektron suatu bentuk molekul didasarkan pada jumlah pasangan elektron bebas (PEB) dan pasangan elektron ikatan (PEI) atau kedudukan elektron. Struktur elektron dapat dilihat dari struktur lewisnya. Prinsip dari teori domain elektron adalah sebagai berikut ini:
- Antar domain elektron yang berada pada atom pusat akan saling tolak menolak, dengan ini maka domain elektron dapat mengatur dan meminimalkan tolakan.
- Kekuatan tolakan dari domain elektron adalah PEB – PEB > PEB – PEI > PEI – PEI. Akibat adanya yang dihasilkan dari perbedaan kekuatan tersebut adalah mengecilnya sudut ikatan pada bentuk molekul.
- Bentuk suatu molekul ditentukan oleh pasangan elektron ikatan / PEI
Berikut ini merupakan Rumus Teori Domain Elektron :
AXmEn
Keterangan :
- A : Atom Pusat
- Xm : Jumlah Domain Elektron Ikatan / PEI
- En : Jumlah Domain Elektron Bebas / PEB
Terdapat 11 bentuk molekul berdasar teori domain elektron, antara lainnya yaitu : segitiga planar (AX3), segi emapt piramida (AX5E), Linear (AX2), T-Shape (Ax3E2) dan lain sebagainya.
Teori Hibridisasi
Teori terakhir yaitu teori hibridisasi, yang mana teori ini menyatakan bahwa suatu ikatan molekul dapat terjadi akibat terbentuknya orbital hibrida yang berada pada sub orbital atomnya. Dari teori hibridisasi ini muncul 5 bentuk molekul yaitu linear (sp), trigonal planar (sp2), tetrahedral (sp3), segitiga berpiramida (sp3d) dan oktahedral (sp3d2).
Nah demikian merupakan pembahasan mengenai bentuk molekul senyawa kimia. Semoga dengan membaca pembahasan diatas, kalian dapat menjadi lebih paham mengenai bentuk suatu molekul senyawa kima. Semoga juga dapat bermanfaat dengan baik untuk anda.
